Fenylalanine is een proteïnogeen, essentieel aminozuur met een aromatische zesring die fungeert als bouwsteen voor veel eiwitten en peptiden.
Daarnaast speelt fenylalanine een belangrijke rol bij het stikstofmetabolisme en kan het in de lever worden omgezet in het proteïnogene aminozuur tyrosine. Fenylalanine en tyrosine spelen een belangrijke rol bij de synthese van insuline, melanine, thyroxine en neurotransmitters dopamine, serotonine en tyramine.
Wat is fenylalanine?
Fenylalanine is een essentieel alfa-aminozuur dat - in tegenstelling tot de meeste proteïnogene aminozuren - niet alleen bioactief is in de L-vorm, maar in beperkte mate ook als enantiomeer in de R-vorm.
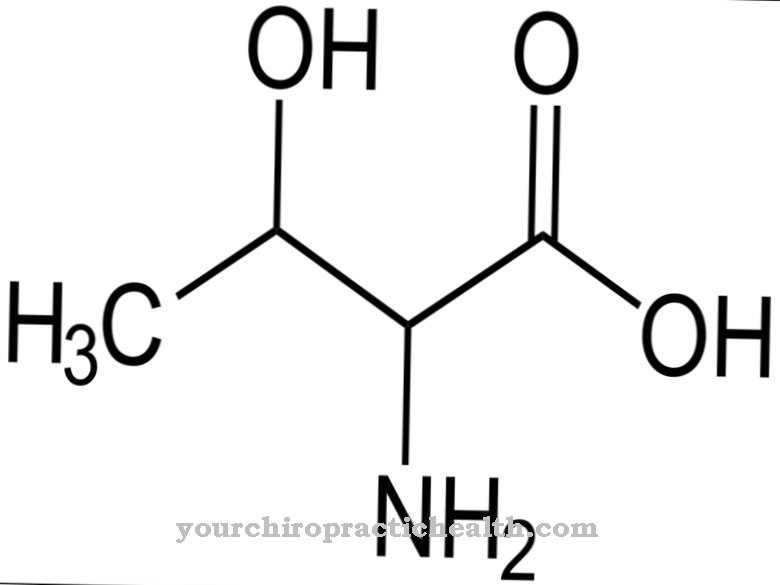
Het R-fenylalanine is biochemisch grotendeels inactief en komt uitsluitend voor bij de kunstmatige productie van het aminozuur, maar de rol van D-fenylalanine bij de controle van bepaalde neurotransmitters binnen het pijncomplex wordt besproken. Als een karakteristiek structureel kenmerk heeft fenylalanine een eenvoudige aromatische zesring (benzeenring) met daaraan een koolwaterstofketen. De chemische structuurformule is C6H5-CH2-CH (NH2) -COOH, waarbij de C6H5-groep de benzeenring aangeeft. Het aminozuur is amfifiel, wat betekent dat het zowel vet- als wateroplosbaar is.
De chemische formule laat ook zien dat fenylalanine uitsluitend bestaat uit koolstof, waterstof, stikstof en zuurstof, stoffen die alomtegenwoordig zijn. Zeldzame metalen, mineralen of sporenelementen maken geen deel uit van het aminozuur. Desalniettemin kan het metabolisme van de mens fenylalanine niet in voldoende mate uit tyrosine synthetiseren, maar is het afhankelijk van opname via voedsel. Fenylalanine is in voldoende hoeveelheden aanwezig in veel dierlijk en plantaardig voedsel, zodat bij een normaal, gemengd dieet - op voorwaarde dat het spijsverteringskanaal normaal wordt opgenomen - niet bang hoeft te zijn voor een tekort aan het aminozuur.
Functie, effect en taken
De belangrijkste functie en taak van fenylalanine is om deel te nemen aan de structuur van veel eiwitten en peptiden. Het is ook betrokken bij de synthese van sommige hormonen die een centrale rol spelen bij de controle van metabolische processen.
Het zijn hormonen zoals adrenaline, noradrenaline, L-dopa, PEA en melanine. Bovendien dient L-fenylalanine als de basisstof waaruit z. B. de boodschappersubstantie dopamine, serotonine, tyramine en andere kunnen worden gesynthetiseerd. L-fenylalanine dient ook als uitgangsmateriaal voor het essentiële aminozuur tyrosine. Hiervoor wordt fenylalanine in de lever in twee stappen omgezet in tyrosine door hydroxylering en door afsplitsing van een watermolecuul. Fenylalaninehydroxylase is het enzym dat de omzetting naar tyrosine katalyseert.
Een alternatieve aanvoer van het eveneens essentiële aminozuur tyrosine kan - net als bij fenylalanine - plaatsvinden via voedselopname. In tegenstelling tot alle andere aminozuren, die alleen een bioactieve werking hebben in hun L-vorm, lijkt de D-enantiomeer van fenylalanine in ieder geval invloed te hebben op de perceptie van pijn. Een mengsel van L- en D-fenylalanine (racemisch mengsel) bleek een analgetisch effect te hebben. Het DL-mengsel blokkeert waarschijnlijk de afbraak van enkefalines - de lichaamseigen opioïden - zodat het pijnstillende effect verlengd en versterkt wordt.
Opleiding, voorkomen, eigenschappen en optimale waarden
Het essentiële aminozuur fenylalanine wordt via de voeding opgenomen. Het is niet gratis, maar meestal als onderdeel van een eiwit of polypeptide in chemisch gebonden vorm. Om het aminozuur beschikbaar te maken voor de stofwisseling, moet het overeenkomstige eiwit eerst tijdens de vertering worden afgebroken en vervolgens met behulp van andere enzymen in de verdere stofwisseling uit de "fragmenten" worden geëxtraheerd.
L-fenylalanine wordt gesynthetiseerd via de zogenaamde shikiminezuurroute. Het is een complexe biokatalytische kettingreactie die autotrofe planten en bacteriën hebben. Het bijzondere van autotrofe organismen is hun vermogen om organisch materiaal te vormen uit uitsluitend anorganisch materiaal. Vrij L-fenylalanine smaakt bitter, terwijl het D-enantiomeer, dat uitsluitend in industriële productie wordt geproduceerd, een zoetige smaak heeft. Het aminozuur is z. B. wordt aangeboden als voedingssupplement en maakt ook deel uit van de kunstmatige zoetstof aspartaam. Biologisch beschikbaar L-fenylalanine wordt in veel voedingsmiddelen in gebonden vorm aangetroffen.
Hun gehalte is bijzonder hoog in gedroogde erwten en sojabonen, in walnoten en pompoenpitten en in verschillende soorten vis en vlees. De behoefte aan fenylalanine is sterk afhankelijk van de aanvoer van tyrosine. Als er geen tyrosine in de voeding zit, heeft het lichaam 38 tot 52 mg per kg lichaamsgewicht nodig. Met een rijk aanbod van tyrosine in de voeding daalt de dagelijkse behoefte tot slechts 9 mg per kg lichaamsgewicht. Levensmiddelen die fenylalanine bevatten, bevatten in de regel ook een overeenkomstige hoeveelheid tyrosine.
De aanbeveling van de FAO / WHO uit 1985 komt neer op een gecombineerde behoefte aan L-fenylalanine en L-tyrosine van 14 mg per kg lichaamsgewicht per dag. Een volwassene met een lichaamsgewicht van 80 kg heeft dus 1.120 mg van beide stoffen per dag nodig.
Ziekten en aandoeningen
Symptomen van een tekort wanneer er permanent onvoldoende fenylalanine en tyrosine in de voeding aanwezig zijn, zijn uiterst zeldzaam, maar kunnen ernstige gevolgen hebben, vooral in het neuronale gebied.
Behalve een verstoring van de synthese van veel hormonen en neurotransmitters, kan het tekort ook worden aangegeven door een verstoring van de myelinisatie van zenuwvezels. Het tegenovergestelde van een tekort, een overconcentratie van fenylalanine (fenylketonurie), kan optreden als gevolg van een genetische stofwisselingsstoornis. De ziekte wordt autosomaal recessief overgeërfd en leidt tot een verminderde aanmaak van het enzym fenylalaninehydroxylase, dat fenylalanine kan omzetten in tyrosine.
De verminderde enzymactiviteit leidt tot een sterke toename van het aminozuur, wat bekend staat als fenylketonurie, omdat de omzetting naar tyrosine ook de afbraakroute is voor fenylalanine. Tegelijkertijd is er een gebrek aan tyrosine omdat het synthesepad geblokkeerd is. Een andere erfelijke ziekte in deze context is het Hartnup-syndroom. Het is een stofwisselingsstoornis die het transport van fenyalanine door het celmembraan verstoort. Dit leidt tot ernstige problemen in het CZS, op de huid en in het spijsverteringskanaal.

.jpg)



.jpg)