Net zo Profage het faag-DNA van gematigde bacteriofagen wordt genoemd wanneer het aanwezig is in de bacteriële gastheercel. Bacteriofagen werden ontdekt door Félix Hubert d’Hérelle in 1917. Het zijn virussen die zich hebben aangepast aan specifieke bacteriën. In het verdere verloop van het onderzoek werd een onderscheid gemaakt tussen lytische faag met hoge virulentie en gematigde faag met stille profaag en lysogene cyclus.
Wat zijn profagen?
De profaag van gematigde bacteriofaag kan als plasmide in de gastheercel aanwezig zijn of in het bacteriële DNA worden geïntegreerd. Hiervoor moet de gematigde faag de lysogene cyclus aannemen wanneer het faag-DNA wordt geïnjecteerd. Er wordt onderscheid gemaakt tussen de lytische cyclus en de lysogene cyclus. Terwijl de lytische cyclus een snelle replicatie en daaropvolgende lysis van de gastheercel veroorzaakt na de injectie van het genetisch materiaal, worden in de lysogene cyclus repressorgenen van de faag in de gastheercel geïnjecteerd om de lytische cyclus te onderdrukken, d.w.z. het snel oplossen van de cel.
De gematigde faag kan schakelen tussen lytische en lysogene cyclus, afhankelijk van de heersende omgevingsomstandigheden. De lytische cyclus verwijst naar de conventionele manier waarop de faaggenen werken in de gastheercel. Snelle replicatie binnen de gastheercel vindt plaats na de injectie van het virale DNA. Nadat naast het virale DNA ook de capside en de staartvezeleiwitten zijn gerepliceerd en talrijke nieuwe virale deeltjes uit de afzonderlijke delen zijn samengesteld, wordt de celwand van de gastheercel afgebroken door lysozym. Als de celwand oplost, komen de nieuwe fagen vrij en kan hun DNA nu in andere bacteriecellen worden geïnjecteerd. Dit proces is in ongeveer een uur voltooid.
Vanwege het grote aantal nieuwe virusdeeltjes wordt deze benadering de "virulente vorm" genoemd. Omdat de celwand van de gastheer wordt vernietigd door middel van lysozym, wordt de term "lytische cyclus" gebruikt. In het geval van gematigde faag hoeft de snelle replicatie en daaropvolgende lysis van de gastheercel niet noodzakelijkerwijs in werking te treden. Afhankelijk van de bestaande omgevingsfactoren kan de gematigde faag schakelen tussen lytische en lysogene cyclus. De lytische cyclus kan worden onderdrukt door repressorgenen te injecteren en de lysogene cyclus kan voor onbepaalde tijd beginnen.
In de lysogene cyclus wordt het genetisch materiaal van de faag ingebracht in het genetisch materiaal van de kiem en kan het hier voor onbepaalde tijd overleven. Het geïnjecteerde genetische materiaal wordt "still" genoemd en wordt gedefinieerd als "profaag". De profaag kan als plasmide in het cytoplasma van de gastheercel liggen of geïntegreerd zijn in het genetisch materiaal van de bacterie.
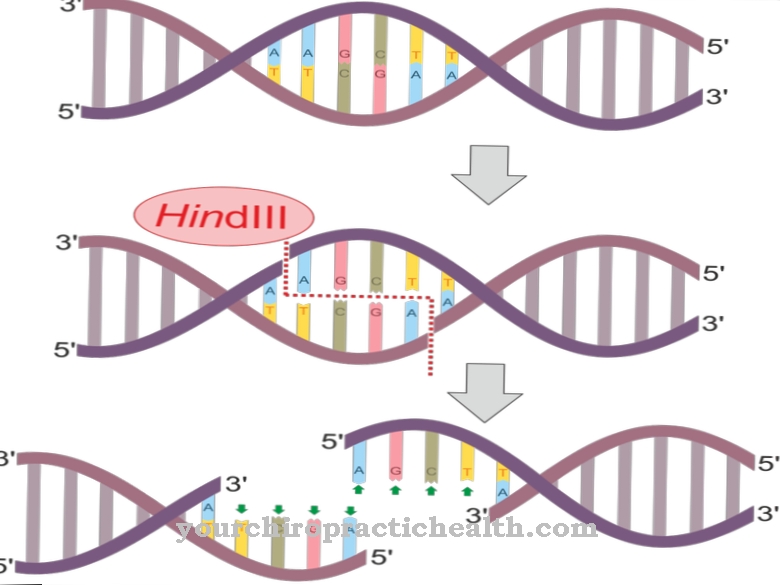
De integratie van het viraal genetisch materiaal vereist een hoge mate van specialisatie. Het genoom van de gematigde fagen kan alleen op bepaalde posities in het bacteriële DNA worden vastgemaakt. Omgekeerd kan het genetisch materiaal van individuele gematigde faagstammen altijd op dezelfde locaties in het bacteriële genoom worden geïdentificeerd.
De succesvolle aanpassing maakt profagen begunstigden van bacteriële celdeling. Wanneer de gastheercel mitose deelt, wordt het virale genetische materiaal doorgegeven. Verdere overdracht naar andere bacteriën kan plaatsvinden door middel van conjugatie. Profagen kunnen zich daarom via verschillende transmissieroutes over hele bacteriestammen verspreiden. Door omgevingsinvloeden zoals UV-licht of bepaalde chemicaliën kan de profaag terugschakelen naar de lytische cyclus en streven naar agressieve replicatie.
De profaag maakt ook gebruik van de transcriptieprocessen van de gastheercel: de geïnjecteerde repressorgenen van de faag worden door bepaalde enzymen van de bacterie als DNA-beschadiging herkend en afgebroken. De afbraak van de repressorgenen is zelfdestructief in de gastheercel. De lytische cyclus kan niet langer worden onderdrukt en de profaag schakelt van de lysogene toestand over naar agressieve replicatie, die eindigt met het daaropvolgende oplossen van de bacteriële celwand.
Voorkomen, distributie en eigenschappen
Fagen zijn zeer gespecialiseerde virussen die zich hebben aangepast aan individuele bacteriestammen. Dus niet elke bacteriofaag heeft toegang tot elke bacterie. Vermenigvuldiging zonder de specifieke gastheercel is niet mogelijk voor de bacteriofaag. Door de hoge mate van specialisatie bevinden bacteriofagen zich op hetzelfde terrein als hun gastheercellen.
Hetzelfde geldt in nog grotere mate voor profagen. Omdat profagen geen conventionele virussen zijn en zichzelf alleen binnen het gastheerorganisme als viraal erfelijk materiaal presenteren, kunnen ze vanwege de definitie alleen niet buiten de toegewezen cellen worden gevonden.
Bovendien moet worden vermeld dat bacteriofagen alleen in zeewater een aantal (10 tot de macht van 30) en dus meer fagen hebben dan levende wezens op de hele planeet. Daarentegen is er een zeer klein aantal van negentien officieel onderzochte bacteriofagen, wat het moeilijk maakt om een precieze uitspraak te doen over het voorkomen.
Betekenis en functie
Faagtherapie werd ontwikkeld in de jaren 1920 en wordt tot op de dag van vandaag met succes toegepast in Oost-Europa om verschillende infectieziekten te bestrijden. De voordelen van faagtherapie liggen voor de hand: bacteriofagen beschadigen alleen individuele bacteriestammen, terwijl antibiotica over het algemeen een schadelijk effect hebben op bacteriën in het lichaam.
De ontdekking van penicilline in de jaren veertig leidde tot het massale gebruik van antibiotica in het Westen en daarmee tot een einde aan het faagonderzoek. De daaropvolgende opbouw van talrijke antibioticaresistenties leidde in de jaren negentig tot een toenemende belangstelling voor bacteriofagen.
Faagtherapie richt zich op bacteriofagen met agressieve virulentie en een uitsluitend lytische cyclus, terwijl gematigde bacteriofagen en profagen tot nu toe slechts een ondergeschikte rol hebben gespeeld.
Ziekten en aandoeningen
Sommige pathogenen kunnen hun virulentie alleen opbouwen door symbiose met profagen. Clostridium botulinum kan het gevreesde botulinumtoxine alleen produceren met behulp van het geïntegreerde faag-DNA. Streptococcus pyogenes kan alleen roodvonk veroorzaken in combinatie met profaag-DNA.
Vibrio cholerae produceert cholera alleen via speciale profagen. Dit toont ook het belang van fagen aan voor de menselijke geneeskunde. Hele bacteriestammen zouden hun pathogene potentieel kunnen verliezen als de verantwoordelijke profagen specifiek zouden kunnen worden uitgeschakeld.


.jpg)

.jpg)
.jpg)


.jpg)