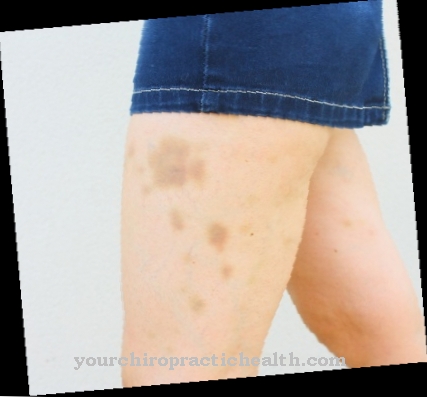
De Enzymvervangende therapie wordt gebruikt om lysosomale stapelingsziekten te behandelen, waarbij het gebrek aan enzymen leidt tot een pathologische ophoping van afbraakproducten in de lysosomen van de cellen.
De ontbrekende enzymen als gevolg van genetische defecten worden gecompenseerd door regelmatige intraveneuze infusies. Omdat de geïnfundeerde synthetische enzymen de bloed-hersenbarrière niet kunnen passeren vanwege hun moleculaire grootte, werkt de therapie alleen voor lysosomale stapelingsziekten die het centrale zenuwstelsel niet aantasten.
Wat is enzymvervangende therapie?

Lysosomen zijn speciale celorganellen waarin vreemde en endogene stoffen worden afgebroken en gedeeltelijk gerecycled. Voor de afbraak en het transport van de stoffen zijn specifieke hydrolyserende enzymen nodig. Dit zijn proteasen, nucleasen, lipasen en transporterende stoffen.
Een aantal bekende genetische defecten kan leiden tot het falen van bepaalde enzymen, zodat sommige afbraakproducten zich ophopen in de lysosomen in pathologische hoeveelheden en zich ophopen totdat ze de extracellulaire matrix, d.w.z. de intercellulaire ruimtes, op een ongecontroleerde manier bereiken. Alle genetische defecten die leiden tot het falen van ten minste één noodzakelijke hydrolase, worden samengevat onder de term lysosomale stapelingsziekte. De enzymvervangende therapie (ERT, enzymvervangende therapie) wordt gebruikt om de ontbrekende endogene enzymen te vervangen door synthetisch geproduceerde enzymen.
Omdat hydrolasen uit relatief grote moleculen bestaan, kunnen ze niet uit de darm worden opgenomen zonder eerst te worden afgebroken en geïnactiveerd, zodat ze alleen via intraveneuze infusie kunnen worden toegediend. De grootte van de enzymmoleculen verhindert echter ook dat de bloed-hersenbarrière wordt overschreden, zodat de therapie alleen effectief kan zijn bij lysosomale stapelingsziekten die het centrale zenuwstelsel (CZS) niet aantasten.
Functie, effect en doelen
Er zijn meer dan 50 verschillende lysosomale stofwisselingsstoornissen bekend, die elk terug te voeren zijn op een monogenetisch defect. De lysosomale stapelingsziekten kunnen worden onderverdeeld in zeven verschillende klassen, afhankelijk van de overmatig opgeslagen stoffen als gevolg van het bestaande enzymdefect.
Mucopolysaccharidosen en oligosaccharidosen zijn vooral geschikt voor een ERT. Het doel van ERT is altijd om het specifieke enzymdeficiëntie te compenseren door middel van de kunstmatig aangevoerde enzymen om de ziekte tot stilstand te brengen of in ieder geval een milder verloop. In detail zijn er vervangende enzymen beschikbaar voor de volgende lysosomale stapelingsziekten:
- Ziekte van Gaucher
- Ziekte van Pompe
- De ziekte van Fabry
- Hurler-Pfaundler-syndroom (mucopolysaccharidose I)
- Ziekte van Hunter (mucopolysaccharidose II)
• Maroteaux-Lamy-syndroom (mucopolysaccharidose VI) • Niemann-Pick B
De ziekte van Gaucher is de meest voorkomende lysosomale stapelingsziekte. Het komt voor in drie verschillende varianten, waarvan er twee ook het zenuwstelsel aantasten. In de niet-neuropathische vorm wordt met name de milt aangetast, wat sterk vergroot en leidt tot secundaire schade zoals bloedarmoede en schade aan het beenmerg. Typische symptomen zijn bot- en gewrichtspijn en stoornissen in de bloedsomloop. De acute neuropathische variant van de ziekte vertoont een ernstig verloop en biedt na de eerste twee levensjaren weinig overlevingskansen.
De stapelingsziekte De ziekte van Pompe wordt veroorzaakt door een tekort aan het enzym alfa-1,4-glucosidase, dat betrokken is bij een groot aantal stofwisselingsprocessen. De ziekte van Pompe leidt tot een enorme vergroting van het hart (cardiomegalie) en hartfalen. Er zijn vroege, serieuze cursussen die in de eerste paar maanden van het leven verschijnen, evenals mildere vormen die pas in latere levensjaren verschijnen.
De ziekte van Fabry wordt veroorzaakt door een X-gebonden genetisch defect, dus alleen jongens en mannen kunnen door de stapelingsziekte worden getroffen. De ziekte leidt meestal tot symptomen in de gevorderde kinderjaren, waaronder pijnaanvallen, keratomen van de huid, nierproblemen en hartspierbeschadiging. Het tekort aan het enzym alfa-galactosidase A leidt tot een ophoping van ceramide-trihexoside, wat de oorzaak is van het opwekken van symptomen die ook het autonome zenuwstelsel kunnen aantasten.
Het is niet ongebruikelijk dat de schade leidt tot een hartaanval, een nierinfarct of zelfs een beroerte. Het Hurler-Pfaundler-syndroom is ook bekend als mucopolysaccharidose, type I en wordt veroorzaakt door een verstoring van het glycosaminoglycaanmetabolisme. De ziekte wordt in verband gebracht met een breed scala aan symptomen, waaronder ernstige mentale stoornissen en ernstige skeletveranderingen. Het ziekteverloop is ernstig, zodat de gemiddelde levensverwachting 11 tot 14 jaar bedraagt. De ziekte van Hunter komt overeen met mucopolysaccharidose, type 2 en wordt - net als de ziekte van Hurler - veroorzaakt door een X-gebonden defect. De ziekte wordt gekenmerkt door verloop van verschillende ernst, variërend van in de vroege kinderjaren tot milde beloop die alleen bij volwassen mannen voorkomt.
Vanwege de meest voorkomende hartsymptomen, zoals hartklepafwijkingen en hartspierproblemen, varieert de levensverwachting van normaal tot licht beperkt. Het Maroteaux-Lamy-syndroom (MPS VI) is een van de mucopolysaccharidosen die worden overgeërfd als een autosomaal recessieve eigenschap omdat het genetische defect dat het veroorzaakt niet op het X-chromosoom zit. De ziekte is zeer zeldzaam, met één geval per 455.000 geboorten. Er zijn milde en ernstige vormen bekend.
Symptomen zijn vergrote lever en milt, carpaal tunnelsyndroom en veranderingen in de hartkleppen. De Niemann-Pick B is een sfingomyeline-lipidose, een van de lysosomale stapelingsziekten en wordt veroorzaakt door een genetisch defect op chromosoom 11. Hoewel type B van de ziekte voornamelijk de lever en milt treft, heeft type A ook aanzienlijke neuronale problemen.
Uw medicatie vindt u hier
➔ Geneesmiddelen tegen pijnRisico's, bijwerkingen en gevaren
Aangezien veel van de lysosomale stapelingsziekten die met enzymsubstitutietherapie kunnen worden behandeld, een ernstig beloop hebben met een overeenkomstig hoger sterftecijfer als ze niet worden behandeld, is het grootste risico bij ERT dat het geselecteerde vervangende enzym niet of slechts te zwak werkt.
Een ander risico schuilt minder in de therapie zelf dan in het feit dat de onderliggende ziekte te laat wordt herkend, waardoor de ERT tijdens de kuur kan stoppen, maar de reeds veroorzaakte schade niet kan terugdraaien. Ongeveer elke tweede behandelde patiënt reageert tijdelijk op de infusies met symptomen zoals koorts en koude rillingen. De redenen hiervoor zijn nog niet helemaal duidelijk. Sommige patiënten reageren door antilichamen te vormen en er zijn gevallen bekend waarin patiënten reageerden met huiduitslag en bronchospasmen.








.jpg)





.jpg)
.jpg)